Влияние добавок к электролиту на газообразование и газовый состав аккумуляторных батарей.
Электролит является одним из четырех основных материалов литий-ионных аккумуляторов, известных как"кровь"литий-ионных аккумуляторов. Электролит в основном состоит из органических растворителей, электролитных солей лития и различных типов добавок. Органический растворитель является основной частью электролита. Обычными растворителями для литий-ионных аккумуляторов являются этиленкарбонат (ЕС ), диэтилкарбонат (ДЕК ), диметилкарбонат (ДМС ), метилэтилкарбонат (ЭМС ) и т. д. Смешанный растворитель ЕС и цепочечного карбоната является отличным электролитом для литий-ионные аккумуляторы, такие как ЕС +ДМС , ЕС +ДЕК и т. д.
LiPF6 является наиболее часто используемой литиевой солью электролита, которая стабильна для отрицательного электрода, обладает высокой разрядной емкостью, высокой проводимостью, низким внутренним сопротивлением и быстрой скоростью зарядки и разрядки. Однако он чрезвычайно чувствителен к воде и фтористоводородной кислоте, склонен к реакциям, неустойчив к высоким температурам. Он разлагается от 80 ℃ до 100 ℃ с образованием пентафторида фосфора и фторида лития. Подходящие добавки могут эффективно уменьшить следовые количества воды и ВЧ -кислоты в электролите, тем самым эффективно ингибируя возникновение реакции гидролиза LiPF6 . В настоящее время проводится много исследований типов добавок, и разные производители имеют разные характеристики. и требования к аккумуляторам.&NBSP ;
Типы выбранных добавок также могут различаться. Как правило, добавки не только уменьшают количество воды и ВЧ в электролите, но также применяются для улучшения стабильности интерфейса, работы при высоких и низких температурах, а также для предотвращения перезарядки и разрядки.&NBSP ;На рис. 1 показаны результаты расчета восстановительного потенциала нескольких распространенных растворителей, добавок и растворенных ионов.【1】.
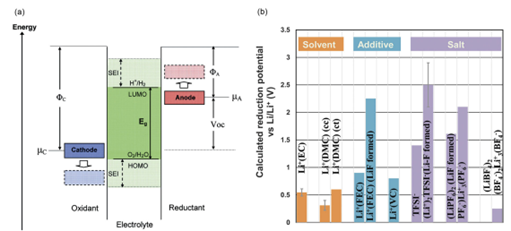
Рисунок 1а.Принципиальная схема энергии разомкнутой цепи электролита&NBSP ;&NBSP ;б.Результаты расчета восстановительного потенциала нескольких распространенных растворителей, добавок и растворенных ионов【1】
Влияние электролитной системы на газообразование литий-ионных аккумуляторов имеет решающее значение, а газообразование внутри аккумулятора напрямую увеличивает риск безопасности при использовании аккумуляторов. Поэтому газообразование аккумуляторов является одним из важных показателей для оценки качества и надежности аккумуляторов. В настоящее время исследования поведения газообразования литий-ионных аккумуляторов в стране и за рубежом в основном сосредоточены на двух аспектах: положительном электроде и электролите. В этой статье анализируется влияние различных электролитных систем на поведение газообразования и состав газа батарея путем объединения положительного электрода НКМ с системой половинных элементов Ли .
Экспериментальное оборудование и методы испытаний
1. Экспериментальное оборудование:Модель ГВМ2200 (ИЭСТ ) с диапазоном температур тестирования от 20 ℃ до 85 ℃, поддерживает двухканальное (2 ячейки) синхронное тестирование. Внешний вид оборудования показан на рисунке 2.

Фигура 2.Внешний вид оборудования ГВМ2200
2. Параметры теста:0,3C CC до 4,4 В при температуре 70 ℃.
3. Метод тестирования:Выберите различные электролитные системы (Электролит1 и Электролит2, где Электролит2 добавляет некоторые добавки поверх Электролита1) и соберите их в однослойную сложенную ячейку в перчаточном боксе. Выполните начальное взвешивание ячейки m0, поместите тестируемую ячейку в соответствующий канал устройства, откройте программное обеспечение MISG , установите соответствующий номер ячейки и параметры частоты дискретизации для каждого канала, и программное обеспечение автоматически считывает изменение объема, тестовая температура и ток, напряжение, емкость и другие данные. Определение состава газа проводили на газовом хроматографе ГХ-2014С. После перезарядки из аккумуляторной батареи в перчаточный бокс отбирали 1 мл газа и тестировали различные концентрации газа с помощью детекторов ТПД и ПИД. Типы измеряемых газов показаны на рисунке 3.
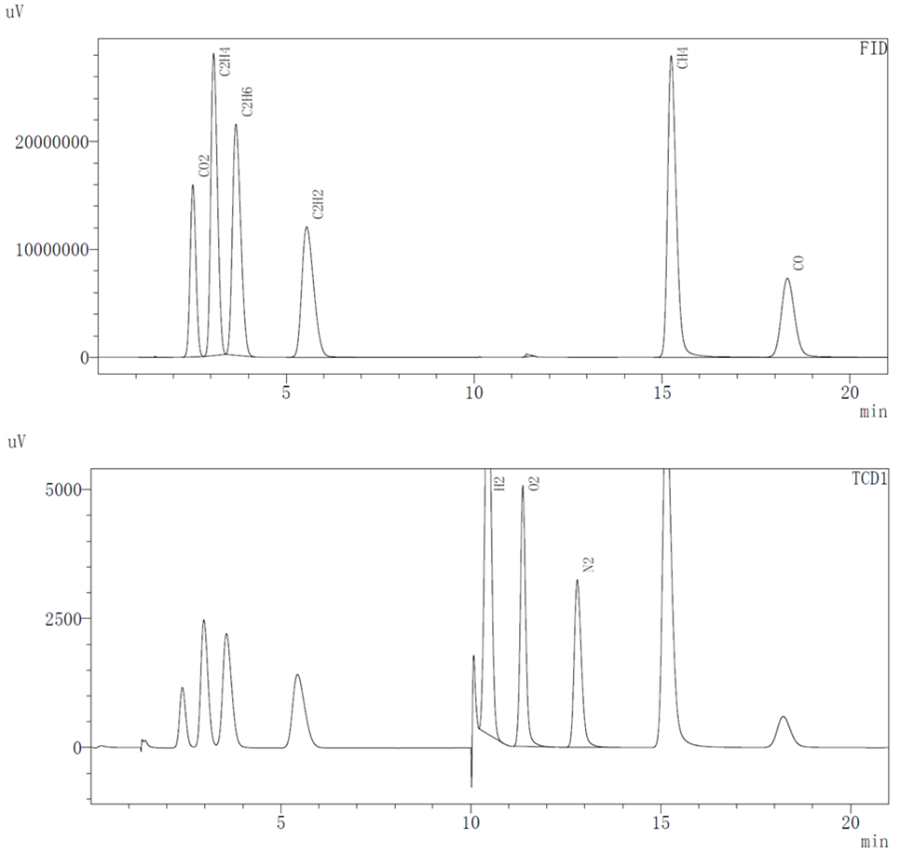
Рисунок 3.Состав газа, который можно проверить с помощью детекторов ПИД и ТПД
Производство газа на месте и анализ состава различных электролитных систем
1. Анализ кривой зарядного напряжения и кривой изменения объема агрегата
Кривые изменения напряжения и удельного объема двух разных электролитных систем показаны на рисунке 4. Из кривых электролита 1 и электролита 2 видно, что существуют значительные различия в кривых изменения зарядного напряжения и объема двух электролитных систем.
Из кривой изменения единичного объема видно, что элемент аккумуляторной батареи системы Электролит1 поддерживает относительно высокую скорость изменения объема на протяжении всей стадии зарядки, в то время как элемент аккумуляторной батареи системы Электролит2 поддерживает относительно низкую скорость изменения объема во время начальной зарядки. этап. Зарядное напряжение достигает примерно 4,2 В, а SOC элемента батареи достигает примерно 80%, после чего скорость изменения объема значительно увеличивается. клетки Ли.
Судя по кривой напряжения, по сравнению с системой Электролит1 среднее зарядное напряжение элемента системы Электролит2 выше. Если игнорировать различия в сборке элементов, добавление добавок в систему электролита2 может вызвать реакцию положительного электрода НКМ элемента с добавками электролита, что приведет к более низкому среднему напряжению элемента.
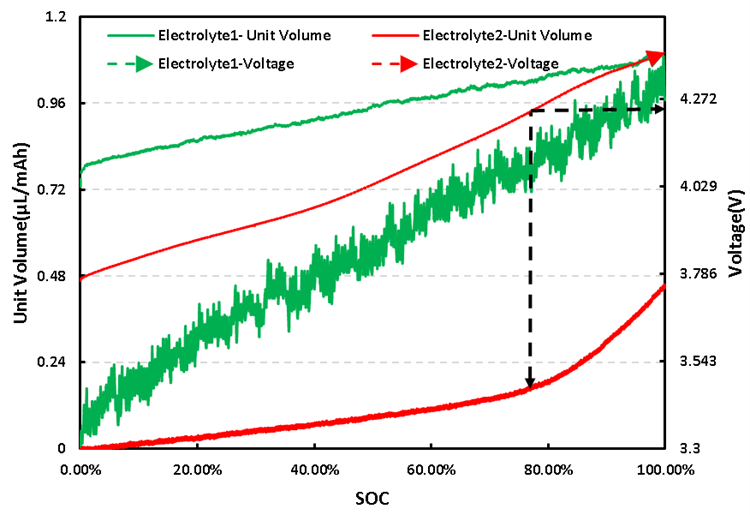
Рисунок 4.Кривая изменения зарядного напряжения и единичного объема двух электролитных систем
2.Анализ компонентов газообразования в ячейках различных электролитных систем.
Газовую хроматографию использовали для анализа газового состава заряженных элементов двух электролитных систем. Отбирали 1 мл газа и проводили качественный анализ с помощью газовой хроматографии. На рис. 5 показан анализ состава газообразных продуктов различных электролитных систем. Сравнительный анализ показал, что по сравнению с системой Электролит1 система Электролит2 с добавками значительно снижает выбросы СО2и увеличение выбросов СО в категории добычи газа.
&NBSP ;Чтобы дополнительно прояснить различия в газообразовании между двумя электролитными системами, был проведен сравнительный анализ их типов и концентраций газообразования. Как показано в таблице 1 и на рисунке 5, СО 2 концентрация системы Электролит1 после зарядки составила 6,949%, а СО2 концентрация системы Электролит2 после добавления добавок была практически нулевой. Согласно соответствующим исследовательским отчетам, СО 2 является основным газом в реакции положительного электрода [2], а газ положительного электрода в основном образуется в результате побочной реакции между материалом положительного электрода и электролитом. Это указывает на то, что добавка в электролите Электролит2 может быть эффективной пленкообразующей добавкой положительного электрода, которая может образовывать стабильную защитную пленку на поверхности положительного электрода, тем самым эффективно уменьшая возникновение побочных реакций между положительным электродом и электролитом. Точно так же уменьшение C2ЧАС4и С2ЧАС2концентрации также связаны с изменением реакции положительного электрода в этой системе.
Для изменений концентрации СО , связанных с реакцией отрицательного электрода, по сравнению с концентрацией СО 0,097% в системе «Электролит 1», концентрация СО в системе «Электролит 2» увеличилась до 6,870% после добавления добавок. Из-за значительного влияния температуры на реакцию газообразования материала отрицательного электрода в системе элементов добавление добавок в систему электролита2 снизит термическую стабильность отрицательного электрода и ускорит протекание побочных реакций при высокие температуры. Кроме того, могут быть разные концентрации других типов газов, что может быть связано с различиями в сборке элементов в дополнение к различиям в электролитных системах.
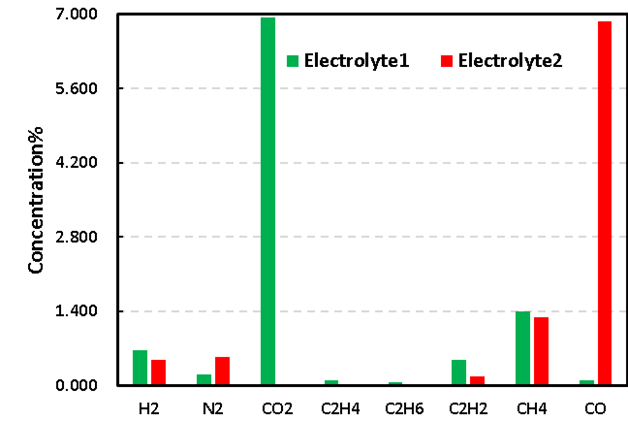
Рис. 5. Сравнение типов газообразования и концентраций в различных электролитных системах.
Таблица 1. Сравнение типов газообразования и концентраций в различных электролитных системах

Суммари
В этой статье используется двухканальный монитор объема производства газа на месте с регулируемой температурой в сочетании с газовой хроматографией для сравнения поведения газа и различий в составе газа НКМ на литиевых батареях при различных системах электролита. Это дополнительно проясняет различия в электрохимической реакции внутри элемента батареи, вызванные добавками, и подтверждает, что эта система анализа может быть эффективным средством для оптимизации состава электролита, оценки и проверки эффективности добавок.
Справочные документы
【1】 Ван А., Кадам С., Ли Х. и др. Обзор моделирования межфазной поверхности твердого электролита анода (СЭИ ) для литий-ионных аккумуляторов [J].
【2】Чен Вэйфэн Исследование и прогнозирование механизма образования газа для гибкой упаковки литий-ионных аккумуляторов [D] Университет Цинхуа, 2012.
【3】 Лян К., Пахира С., Ян З. и др. Нанопористый слой СС , легированный серой, на пути к высокоэффективному выделению водорода в рН-универсальном электролите [J]. Катализ АСУ, 2018, 9(1).
【4】Цуй Шэнъюнь , Электрохимическая окислительная полимеризация бифенила и трифенила в органических растворителях [J], Электрохимия, 2000, 6 (4): 428-433.
